アーティクルサマリー
BSCCI vol.8
急性冠症候群に対するSYNERGY留置後の
血管内皮前駆細胞の動員と血管修復
背景
薬剤溶出型ステント(DES)技術の進歩によって、標的病変における再血行再建率は低下したが、第2世代DESであっても、ステント留置後の血管修復は不完全であるという懸念が依然として残っている。ステント留置後の血管修復には、ステントストラットの再内皮化と新生内膜の被覆が不可欠である。この血管修復過程において、ステント留置後の炎症反応が誘因となり、血管内皮前駆細胞(CD34+/KDR+)と平滑筋前駆細胞がステントで損傷した血管部位へと動員することが報告されている。
第3世代DESのSYNERGY™は、ストラット厚が74μmのバルーン拡張型プラチナ・クロム合金製ステントであり、ステント表面の血管壁側に塗布された超薄(4μm)の生体吸収性PLGAポリマーからエベロリムスが溶出され、その生物学的および薬理学的特性によって最適な血管治癒を行うことを目的として開発された。*
本研究では、急性冠症候群(ACS)に対する緊急経皮的冠動脈インターベンション(PCI)ステント留置後のCD34+/KDR+の動態と血管修復過程を、SYNERGYとステントプラットフォームの形状が同じであるが、ストラット厚とアブルミナルコーテイングが異なる第2世代DESのPROMUSPREMIERで比較検討した。
試験デザイン
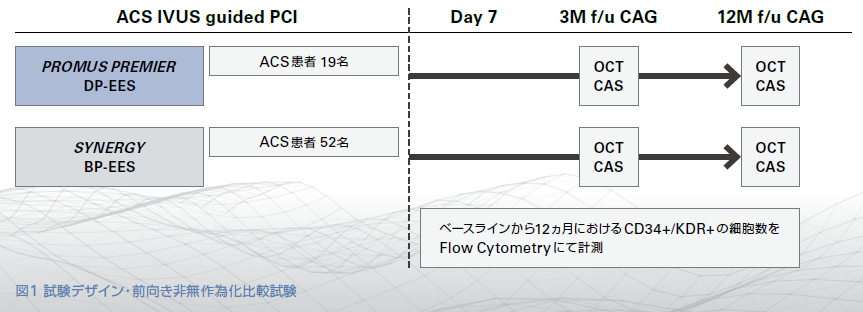
方法
① 末梢血中CD34+/KDR+の測定
ステント留置前(ベースライン)、留置後7日目、3ヵ月目、12ヵ月目に末梢血を採取し、Flow Cytometryを用いて循環血中のCD34+/KDR+細胞数を測定した。
② 光干渉断層法(OCT)による解析
留置後3ヵ月目と12ヵ月目にOCTを施行し、OCT断面画像から非被覆ストラットや圧着不良ストラットを含むすべてのストラットの新生内膜被覆を評価し、平均新生内膜厚を算出し。
③ 冠動脈内視鏡(CAS)検査による解析
留置後3ヵ月目と12ヵ月目に非閉塞型血管内視鏡システムを用いてCAS検査を行った。ストラットの新生内膜被覆度を4段階に分類した。(Grade 0: 新生内膜の被覆なし Grade1: 新生内膜に薄く覆われている Grade 2: 新生内膜によって被覆されているが、ステントが透見できる Grade 3: 新生内膜によって完全に被覆され、ステントは観察できない)
結果および考察
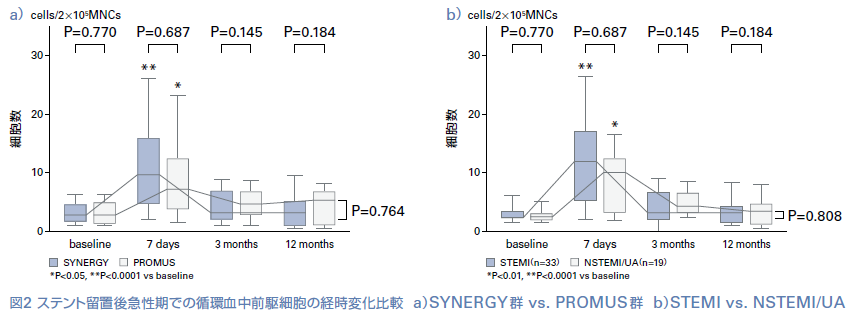
① 末梢血中CD34+/KDR+細胞の動態ベースラインに比べ、7日目のCD34+/KDR+細胞数はSYNERGY群で有意に増加していた(P<0.0001)(図2a)。
また病態別にみるとSTEMI患者(33例)ではベースラインに比べ、CD34+/KDR+細胞が7日目に有意に増加した(P<0.0001)(図2b)。
② OCTおよびCASの所見
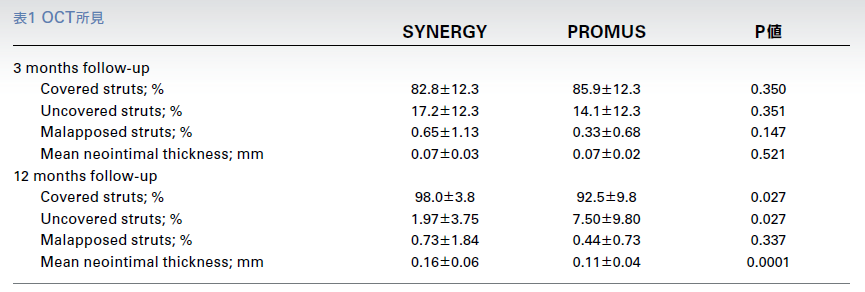
OCT所見では、3ヵ月目の全ストラットにおける非被覆ストラットの割合と平均新生内膜厚は両群間で同等であったが、12ヵ月目になるとSYNERGY群ではPROMUS群と比較して非被覆ストラットの割合が有意に少なく(P<0.05)、平均新生内膜厚が有意に大きかった(P<0.001)(表1)。
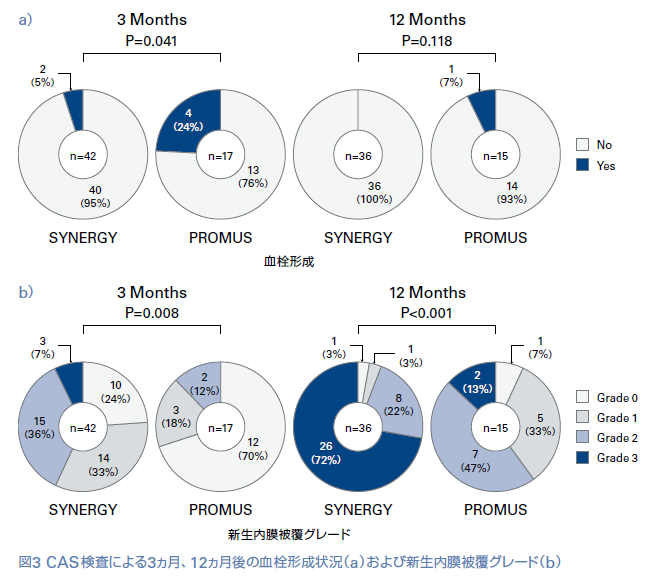
CAS所見では、SYNERGY群はPROMUS群よりも3ヵ月目の新生内膜被覆度が有意に高く(P=0.008)、血栓形成率が有意に低かった(P=0.041)。12ヵ月目の新生内膜被覆度もSYNERGY群がPROMUS群より高く(P<0.001)SYNERGY群では血栓形成症例は認めなかった(図3)。
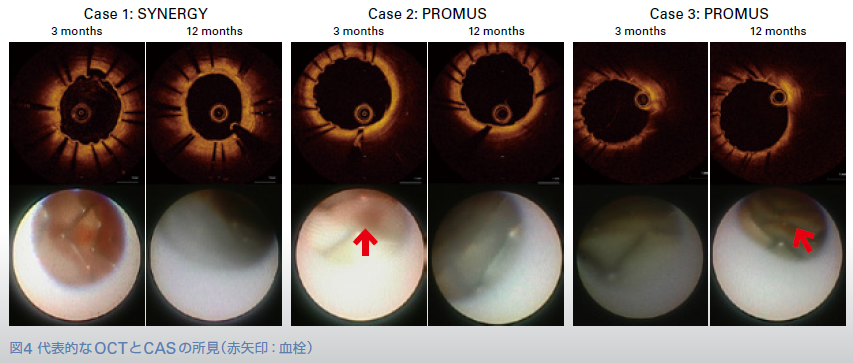
代表的なOCTおよびCAS所見を図4に示す。Case1:3ヵ月目にuncoveredやmalapposed strutsを認めたSYNERGY症例である。間隙に血流を認める程であったが、12ヵ月目には新生内膜の被覆が確認された。Case2:PROMUS症例である。3ヵ月目でuncovered strutsに壁在血栓が確認され、12ヵ月目でも被覆は不十分であった。Case3: PROMUS症例である。12ヵ月目でも血管修復が遅延し壁在血栓と黄色プラークが確認された。
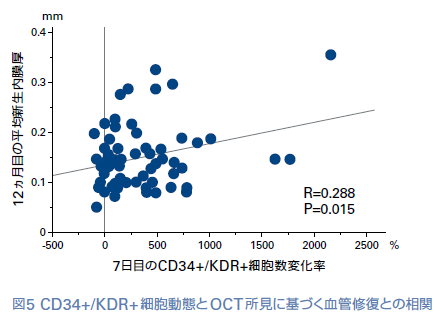
両群を合わせた71例の患者において、ベースラインと比べた7日目のCD34+/KDR+ 細胞数変化率と12ヵ月目のOCTによる平均新生内膜厚は有意な相関を示した(R=0.288、P=0.015)(図5)。CD34+/KDR+ 細胞動態とOCTベースの新生内膜厚の相関関係の結果は、血管内皮前駆細胞がステント留置後の血管傷害部位における創傷修復の役割を強く担っている可能性がある。
結論
論文ポイント
- CD34+/KDR+細胞数の変化率と新生内膜厚は相関する。
- CD34+/KDR+細胞はステント留置部位での血管修復反応において重要な役割を担っている。
- SYNERGYステント(BP-EES)はPROMUS PREMIERステント(DP-EES)よりも血管内皮前駆細胞(CD34+/KDR+)の動員がより顕著であり、その後の新生内膜形成とステント被覆率が優れている。
*ストラット厚が74μmのステントはSYNERGY™のsmall vesselモデルになります
承認番号・販売名
販売名 : シナジー ステントシステム
医療機器承認番号 : 22700BZX00372000
販売名 : プロマス プレミア ステントシステム
医療機器承認番号 : 22600BZX00181000











 PDFを開く
PDFを開く