アーティクルサマリー
BSCCI vol.3
Aspirin-Free Prasugrel Monotherapy Following Coronary Artery Stenting in Patients With Stable CAD:
背景
試験Design(Figure 15)
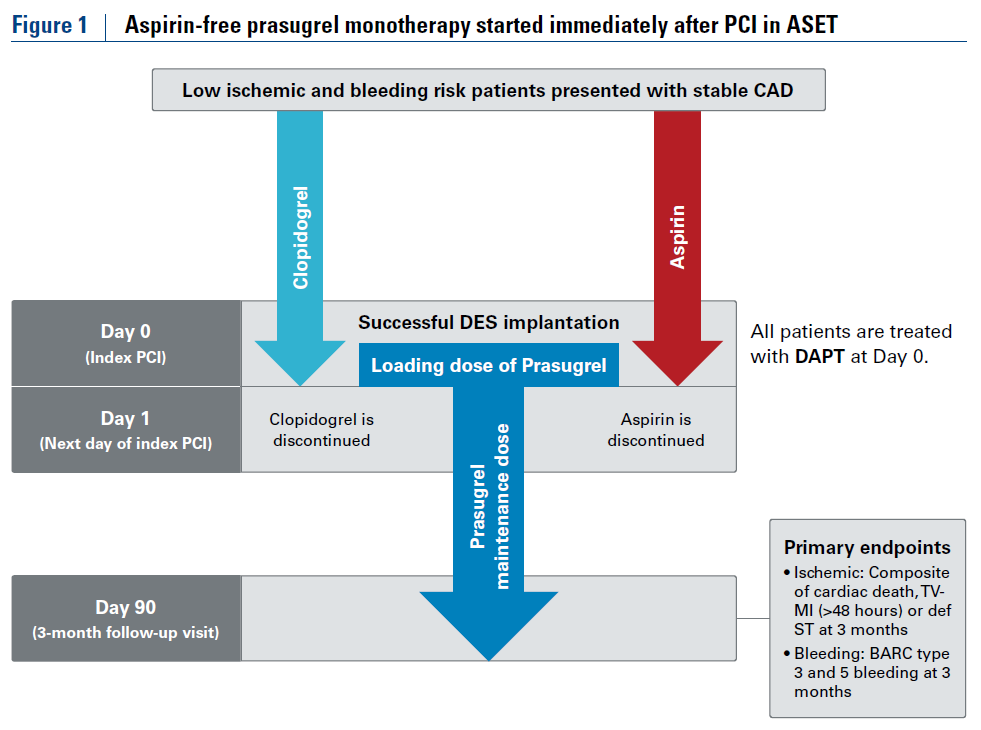
結論、考察
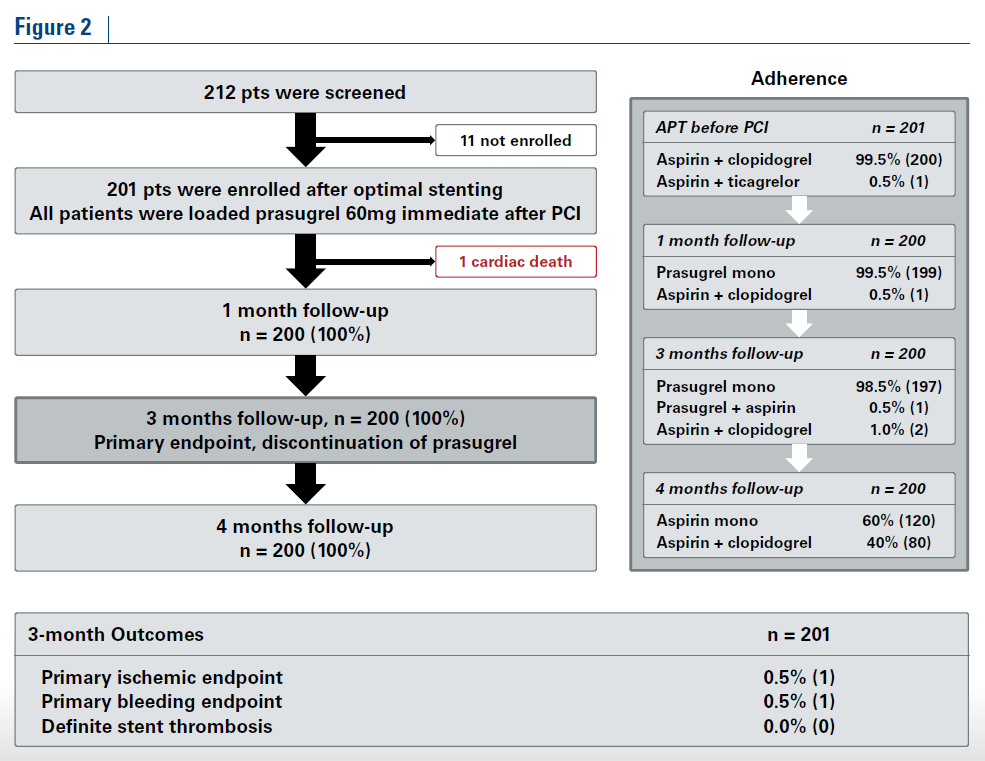
2018年2月から2019年5月の間に201人の患者が登録された。プラスグレル単剤療法は98.5%の患者において達成された。Primary ischemic endpointとPrimary bleedingendpointは1件発生した(0.5%、脳出血からの死亡[手技との関連が否定できず心臓死と判定])。Definite stentthrombosisは1例も発生しなかった(Figure 2 5)。
この試験は、世界で初めて前向きにPCI後のAspirin-freeprasugrel monotherapyを評価し、解剖学的に複雑性の低い患者群ではあるが安全性、実現可能性を示した点が特徴である。短期(またはNo)DAPT後のP2Y12阻害薬単剤療法は従来の抗血小板療法と比較し重篤な出血を減少させ虚血性イベントを増加させないことが知られているが3、その恩恵が最も期待できるのが中等度から高度の出血リスクを要する患者群である。しかし、これらの患者群は虚血性イベントリスクも高く、初めてAspirin-free prasugrel monotherapyを導入するにはリスクが高すぎると考えられた。そのため、本試験では多くの除外基準を設けることで出血リスク、虚血性イベントリスクともに低い患者群を対象とした上、Definite stent thrombosisの発生数に基づいたStopping ruleを設定することで患者の安全性を担保した。本試験の結果から、Aspirin-free prasugrelmonotherapyの安全性が示唆され今後無作為化比較試験において従来の抗血小板療法との比較が可能になると思われる。ただし、中等度から高度の出血リスクを要する患者群においてはComplex PCI featuresや急性冠症候群の合併が多く、無作為化比較試験に進む前にこれらの患者群におけるAspirinfreeprasugrel monotherapyの安全性(特に急性期のstent thrombosis)を確認する必要があると思われる。
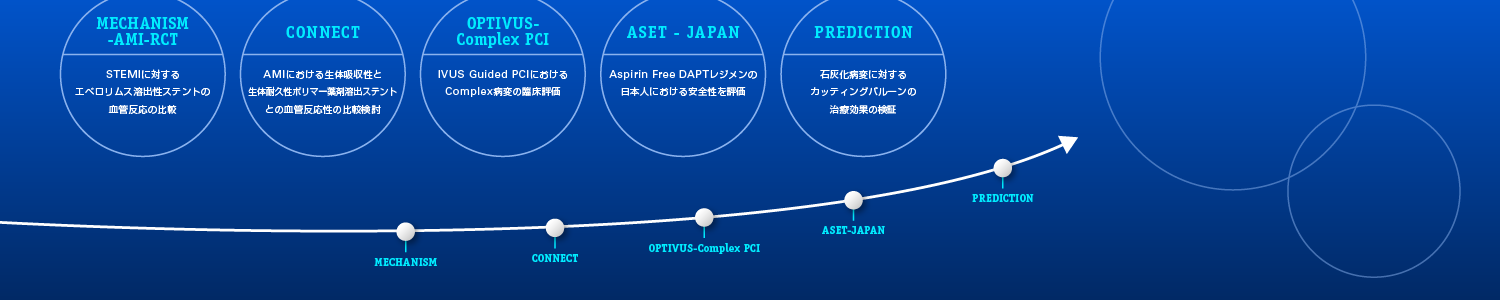
今後始まる臨床試験
本試験はブラジルで行われており、プラスグレルは負荷投与が60mg、維持用量が10mg/日と本邦における用量と異なる(負荷投与:20mg、維持用量:3.75mg/ 日)。本邦において、低用量プラスグレルの安全性、有効性については安定狭心症、急性冠症候群いずれの患者群においても証明されており、日常臨床においても広く用いられている6, 7。しかし、低用量プラスグレルのPCI後1ヶ月以内の単剤投与におけるDataは乏しく国際用量とは別の検討が必要であると思われる。そこで本邦において低用量プラスグレルを用いたASET Japan試験(CRB4180003)が進行中である。基本的なDesignはASET Brazilと同様であるが、安定狭心症患者における安全性が確認された後に非ST上昇型急性冠症候群を対象とした2nd phaseを設けていることが特徴であり、安全性が証明されればよりスムーズに大規模無作為化臨床試験に移行することができると思われ結果が期待される。
References
- Byrne RA, Serruys PW, Baumbach A, Escaned J, Fajadet J, James S, Joner M, Oktay S, Juni P, Kastrati A, Sianos G, Stefanini GG, Wijns W, Windecker S. Report of a European Society of Cardiology-EuropeanAssociation of Percutaneous Cardiovascular Interventions task force on the evaluation of coronary stents in Europe: executive summary. Eur Heart J 2015;36(38):2608-20.
- Valgimigli M, Costa F, Lokhnygina Y, Clare RM, Wallentin L, Moliterno DJ, Armstrong PW, White HD, Held C, Aylward PE, Van de Werf F, Harrington RA, Mahaffey KW, Tricoci P. Trade-off of myocardial infarctionvs. bleeding types on mortality after acute coronary syndrome: lessons from the Thrombin Receptor Antagonist for Clinical Event Reduction in Acute Coronary Syndrome (TRACER) randomized trial. EurHeart J 2017;38(11):804-810.
- Giacoppo D, Matsuda Y, Fovino LN, D'Amico G, Gargiulo G, Byrne RA, Capodanno D, Valgimigli M, Mehran R, Tarantini G. Short dual antiplatelet therapy followed by P2Y12 inhibitor monotherapy vs.prolonged dual antiplatelet therapy after percutaneous coronary intervention with second-generation drug-eluting stents: a systematic review and meta-analysis of randomized clinical trials. Eur Heart J 2020.
- Kogame N, Modolo R, Tomaniak M, Cavalcante R, de Martino F, Tinoco J, Ribeiro EE, Mehran R, Campos CM, Onuma Y, Lemos PA, Serruys PW. Prasugrel monotherapy after PCI with the SYNERGY stent inpatients with chronic stable angina or stabilised acute coronary syndromes: rationale and design of the ASET pilot study. EuroIntervention 2019;15(6):e547-e550.
- Kogame N, Guimaraes PO, Modolo R, De Martino F, Tinoco J, Ribeiro EE, Kawashima H, Ono M, Hara H, Wang R, Cavalcante R, Moulin B, Falcao BAA, Leite RS, de Almeida Sampaio FB, Morais GR,Meireles GC, Campos CM, Onuma Y, Serruys PW, Lemos PA. Aspirin-Free Prasugrel Monotherapy Following Coronary Artery Stenting in Patients With Stable CAD: The ASET Pilot Study. JACC CardiovascInterv 2020;13(19):2251-2262.
- Isshiki T, Kimura T, Ogawa H, Yokoi H, Nanto S, Takayama M, Kitagawa K, Nishikawa M, Miyazaki S, Ikeda Y, Nakamura M, Saito S, Investigators PR-E. Prasugrel, a third-generation P2Y12 receptor antagonist,in patients with coronary artery disease undergoing elective percutaneous coronary intervention. Circ J 2014;78(12):2926-34.
- Saito S, Isshiki T, Kimura T, Ogawa H, Yokoi H, Nanto S, Takayama M, Kitagawa K, Nishikawa M, Miyazaki S, Nakamura M. Ef cacy and safety of adjusted-dose prasugrel compared with clopidogrel inJapanese patients with acute coronary syndrome: the PRASFIT-ACS study. Circ J 2014;78(7):1684-92.
承認番号・販売名
販売名 : シナジー ステントシステム
医療機器承認番号 : 22700BZX00372000











 PDFを開く
PDFを開く