アーティクルサマリー
BSCCI vol.10
ST上昇型急性心筋梗塞に対する第三世代薬剤溶出ステント
または第二世代薬剤溶出ステントによる治療後早期および中期の
血管反応に関する血管内視鏡を用いた比較:
MECHANISM AMI RCTの事前設定サブ解析
背景
血管壁側のみに生体吸収性ポリマーをコーティングした(アブルミナルコーティング)新世代薬剤溶出型ステント(第三世代DES)は、薬剤溶出が終わるとすぐにポリマーが完全に吸収されるため、全周性に耐久性ポリマーをコーティングした第二世代薬剤溶出ステント(第二世代DES)に比べてポリマーの曝露が少なくなる。またアブルミナルコーティングテクノロジーにより、組織とポリマーの接触面積が減少する。これらの特徴は、慢性的な炎症の惹起や血栓形成促進などといったポリマー残存に伴う長期的な欠点を克服し、結果として長期の追跡調査でステント関連の有害事象を減少させる可能性がある。一方で、特に血栓性の高いST上昇型急性心筋梗塞(STEMI)の責任病変に留置する場合、金属ストラットを生体適合耐久性ポリマーで覆うことで急性期の血栓形成を抑制している第二世代DESに比べて、第三世代DESが生体吸収性ポリマーのアブルミナルコーティングだけで早期および中期のステント不全を防ぐことができるかは不明である。
血管内視鏡(CAS)は、新生内膜被覆度、血栓の有無、動脈硬化性病変を表す黄色プラークを評価することができ、ステントストラットの新生内膜の色調から、健康な内皮とフィブリンや血栓の沈着を容易に区別することできる。しかし、CASは本邦でのみ利用可能であり、これまでに無作為化比較試験で採用されたことはない。
我々は、STEMI責任病変における第三世代DESと第二世代DESの早期および中期の血管治癒反応を連続画像評価により比較する多施設共同前向き無作為化比較試験(MECHANISM-AMI RCT)を実施した。本稿では、その事前設定サブ解析であるCASコホートの成績を報告する。
試験デザイン
対象患者:
MECHANISM-AMI RCTは、前向き、多施設共同、無作為化、非盲検、並行群間、標準治療対照、非劣性試験であり、STEMIのためDESによる経皮的冠動脈インターベンション(primary PCI)を施行する20~85歳の成人患者120例を第三世代DES群(60例)と第二世代DES群(60例)に分け、血管治癒反応を比較した。本研究では、この登録患者のうち、大阪警察病院で登録されたCASコホート20例(各群10例)を対象に事前設定サブ解析を実施した。無作為化はウェブベースの割り付けシステムで行い、年齢、性別、糖尿病の有無で層別化した。
方法:
① 手技
STEMI責任病変に対して、第二世代DESまたは第三世代DESを用いてprimary PCIを施行した。
② 血管内視鏡検査
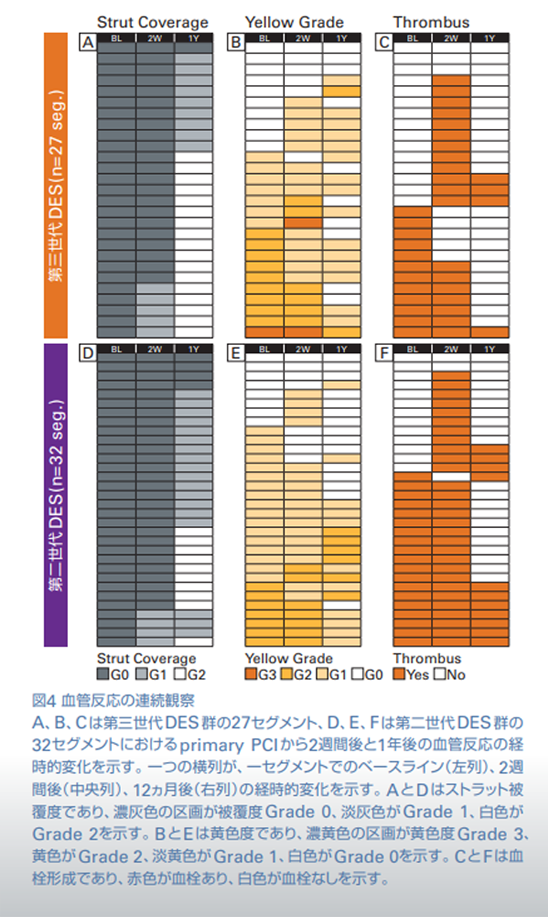
ベースライン、留置2週間後、12ヵ月後に、CASを用いて血管治癒反応を評価した。すべてのステントについて、近位部、中間部、遠位部の各セグメントで新生内膜被覆度、黄色度、血栓の有無を評価した。新生内膜被覆度は3つのGrade(0:被覆なし、1:被覆不良、2:完全被覆)に分類した。黄色度は、標準色との比較により4つのGrade(0:白色、1:淡黄色、2:黄色、3:濃黄色)に分類した。
長期追跡調査(12ヵ月)時点の最適な血管治癒反応を、1)黄色度がGrade 1以下、2)血栓なし、3)新生内膜被覆度がGrade 1以上、と定義した。
③ 評価項目
本サブ解析の主要評価項目は、ステント留置から2週間後のCASによる主要新生内膜被覆度、主な副次評価項目は、留置から2週間後の最大黄色度と血栓の有無、留置から12ヵ月後の新生内膜被覆度、黄色度、血栓の有無、最適な血管治癒反応(Optimal Healing)とした。
結果
① 患者背景
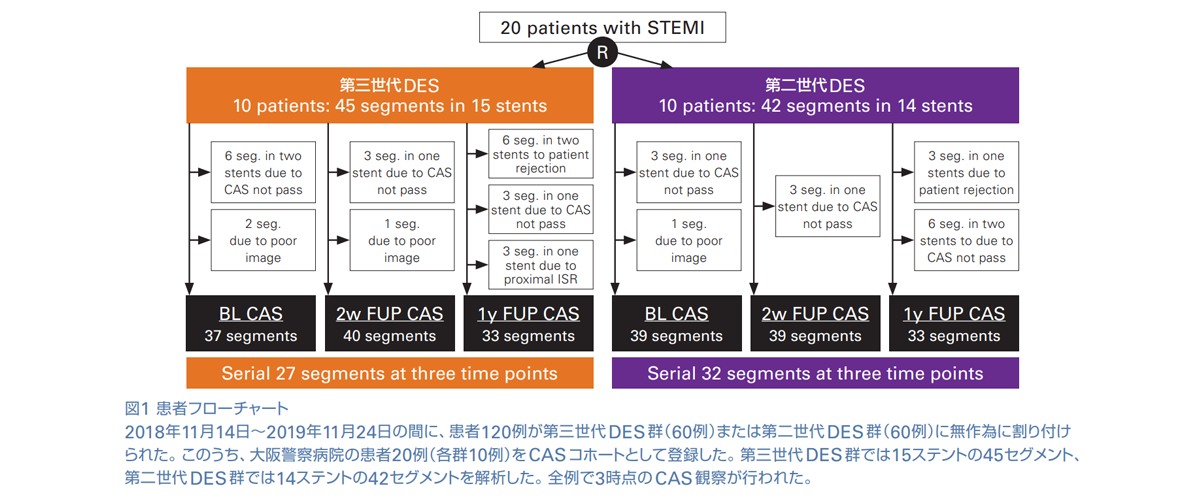
MECHANISM-AMI RCTの対象患者のうち、CASコホートとして大阪警察病院の患者20例が登録された(図1)。第三世代DES群10例(年齢中央値72歳、女性40.0%)では15ステントの45セグメント、第二世代DES群10例(年齢中央値68歳、女性20%)では14ステントの42セグメントが解析された。全患者に高血圧症と脂質異常症の既往、約半数の患者に糖尿病の既往があった。
② 血管内視鏡所見
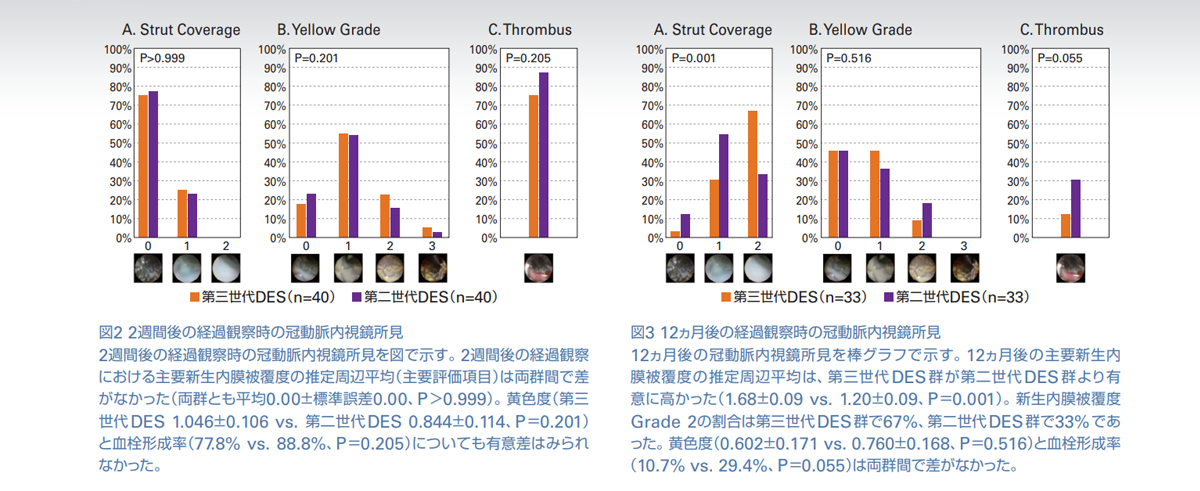
留置から2週間後のCAS所見(図2)では、主要新生内膜被覆度の推定周辺平均は両群間で差がなく(両群で0.00±0.00、P>0.999)、黄色度(第三世代DES 1.046±0.106 vs. 第二世代 DES 0.844±0.114、P=0.201)と 血栓形成率(77.8% vs. 88.8%、P=0.205)も有意差を認めなかった。
留置から12ヵ月後のCAS所見(図3)では、主要新生内膜被覆度の推定周辺平均は、第三世代DES群が第二世代DES群より有意 に 高 かった(1.68±0.09 vs. 1.20±0.09、P=0.001)。新生内膜被覆度Grade 2の割合は、第三世代DES群 で67%、第二世代 DES 群 で33%で あった。黄色度(0.602±0.171 vs. 0.760±0.168、P=0.516)と血栓形成率(10.7% vs. 29.4%、P=0.055)は両群間で有意差はなかったが、血栓形成率は第三世代DES群で低い傾向にあった。
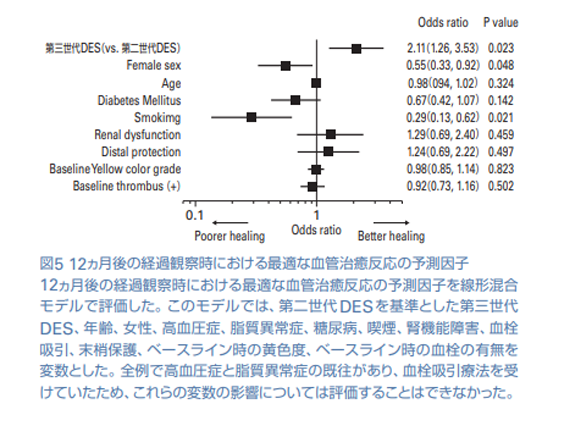
新生内膜被覆度、黄色度、血栓形成の経時的変化を図4に示す。全体として、ハイリスクとされる脆弱性プラーク(黄色度がGrade 2以上)は12ヵ月後には安定していたが、2週間後はまだ安定していなかった。血栓形成は、2週間後はほぼすべてのセグメントで観察されたが、12ヵ月後には消失していた。Optimal Healingの反応が認められた割合は、第三世代 DES 群が第二世代 DES 群よりも高かった(85.2% vs. 53.1%、調整オッズ比2.11、95%CI 1.26~3.53、P=0.023)。女性であることと喫煙は不良な血管治癒反応と関連していた(図5)。
③ 臨床成績
本研究の対象患者では、死亡、心筋梗塞、ステント血栓症は観察されなかった。第三世代DES群の1例が標的病変の再灌流を経験したが、虚血症状は認めていなかった。第二世代DES群では、Bleeding Academic Research Consortiumのタイプ3イベントが2例発生した。
考察
MECHANISM AMI RCTの事前設定サブ解析の結果、第三世代DESと第二世代DESの留置から2週間後の新生内膜被覆度のCAS所見は同等であった。新世代DESは、ポリマーの種類やコーティング方法の面で技術的改良が行われているが、少なくとも留置から2週間後の時点では血管治癒反応に有意差を認めなかった。
12ヵ月後の経過観察では、第三世代 DES は第二世代DESよりも新生内膜被覆度が良好であり、治療した血管の内腔面積も損なわれていなかった。本研究では、第三世代DESがステント留置から12ヵ月後の最適な血管治癒反応の独立した予測因子であることが明確に示され、それには血管壁側コーティングと生体吸収性ポリマーによる薬物放出の制御による血管治癒の促進が関与していると考えられた。
CASによる連続観察では、脆弱性プラークは2週間後の時点では変化がなかったが、12ヵ月後には安定していることが観察された。また、血栓については、2週間後の時点で大半のセグメントで認め、1年の時点では消失していたことから、2週間後の血栓形成は血管治癒の自然経過の最初のステップであることが示唆された。
結論
論文ポイント
- 血管内視鏡による観察では、ステント留置後2週間の時点では、第二世代DESと第三世代DESともに、新生内膜による被覆はほとんど認められないことが示された
- 1年経過時の新生内膜被覆度は、第三世代DESは第二世代DESに比べて有意に高いことが確認された
- 血管治癒過程の経時的検討では、2週間でステント周囲の血栓形成は進行するが、1年経過時で消失していた。これは正常な血管治癒プロセスの一つの過程であると推察される
- 第三世代DESは第二世代DESと比べて、1年フォローアップ時点でのOptimal Healingに強く関連する因子であることが示された
承認番号・販売名
医療機器承認番号 : 22700BZX00372000











 PDFを開く
PDFを開く