WATCHMAN FLX™
Dispositivo de Oclusão de Apêndice Atrial Esquerdo
Construído sobre o dispositivo de LAAC [Left Atrial Appendage Closure - Oclusão de Apêndice Atrial Esquerdo] mais estudado e implantado do mundo, o WATCHMAN FLX é projetado para avançar o desempenho e a segurança do procedimento ao mesmo tempo em que expande a população de pacientes que pode receber o tratamento.
Acesse o portal para pacientes
Explorar
Baixe o material de apoio
Dispositivo de LAAC WATCHMAN FLX

Estudo Clínico PINNACLE FLX

APRESENTAÇÃO DOS ÚLTIMOS AVANÇOS DO PINNACLE FLX
Avaliação de Resultado Primário de um Dispositivo de LAAC da Próxima Geração: O Ensaio PINNACLE FLX
apresentado por Dr. Shephal K. Doshi
8 de maio de 2020
HRS 2020 SCIENCE
Desenho do Estudo
- Ensaio não randomizado, de braço único, com 400 pacientes em 29 locais dos EUA avaliando o WATCHMAN FLX quanto a não inferioridade a metas de desempenho de segurança e eficácia com base no dispositivo WATCHMAN™.
- Acompanhamento: 45 dias (+TEE [Transesophageal Echocardiography - Ecocardiografia Transesofágica]), 6 meses, 12 meses (+TEE), 18 meses, e 24 meses
- Características do Paciente: Média de CHA2DS2-VASc de 4,2±1,5, Média de HAS-BLED de 2,0±1,0
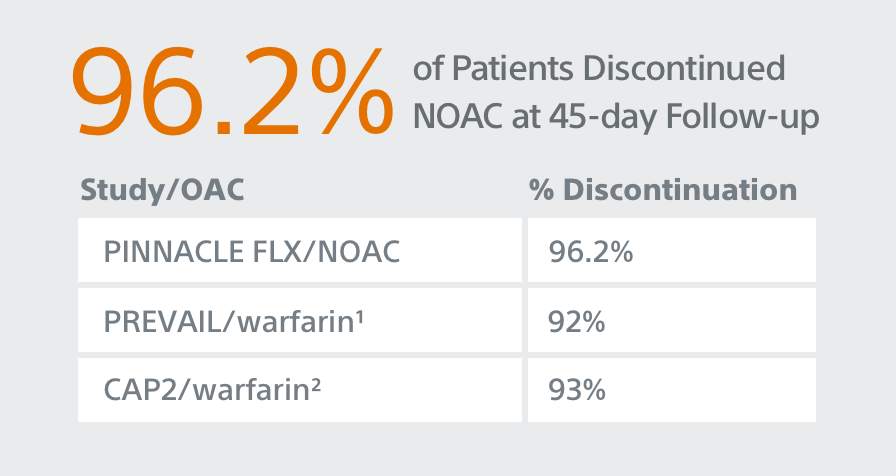
- Regime Medicamentoso Pós Implante: NOAC/AAS por 45 dias, Clopidogrel/AAS até 6 meses, AAS após 6 meses
- Desfecho de Segurança Primário: Morte por todas as causas, derrame isquêmico, embolia sistêmica ou eventos adversos relacionados ao dispositivo ou ao procedimento exigindo cirurgia ou intervenção endovascular em até 7 dias após o procedimento ou por alta hospitalar, qual for posterior.
- Desfechos de Eficácia Primário: A taxa de oclusão de LAA eficaz definida como qualquer fluxo peri-dispositivo ≤5mm demonstrada por TEE aos 12 meses
- Desfecho de Eficácia Secundário: A ocorrência de derrame isquêmico ou embolia sistêmica aos 24 meses a partir do momento do implante.
- Os critérios de inclusão/exclusão são consistentes com os critérios de inclusão/exclusão do estudo clínico WATCHMAN. Os pacientes devem ser elegíveis para NOAC de curto prazo vs. varfarina em estudos clínicos anteriores.
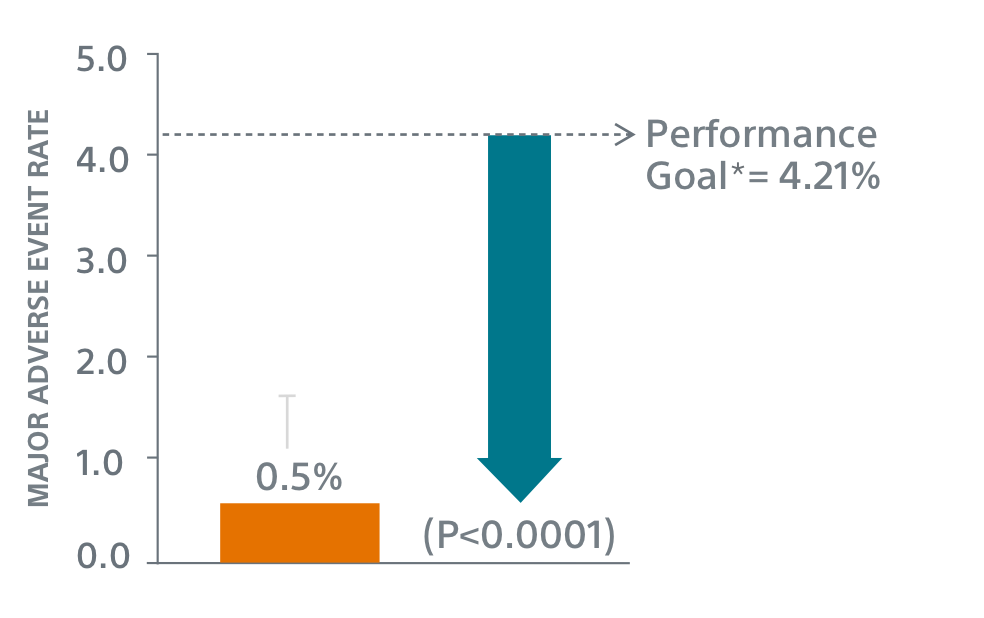
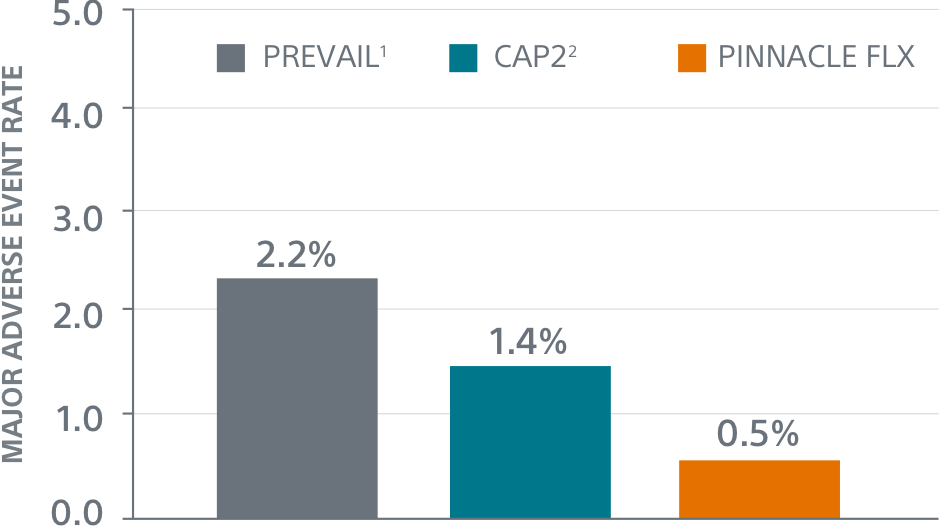
Desfechos de Segurança Primários

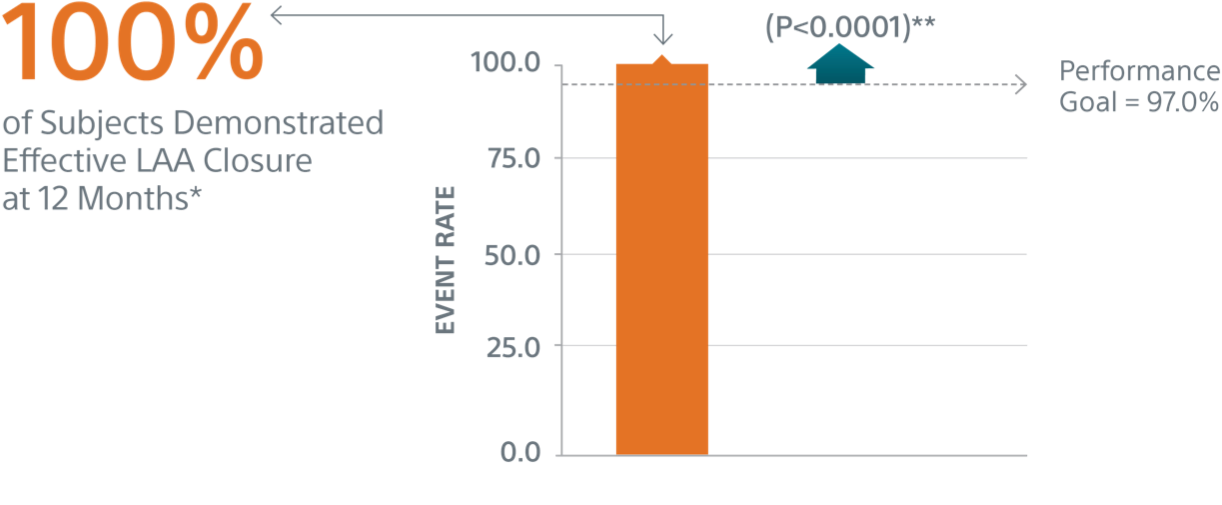
Desfechos de Eficácia Primários
A taxa de oclusão de LAA eficaz definida como qualquer fluxo peri-dispositivo ≤5mm demonstrada por TEE aos 12 meses.
**Meta de desempenho com base nas taxas observadas em PREVAIL(1) e CAP2(2), menos um delta clinicamente relevante
Projetado para Tratar a Maior Gama de Anatomias de Paciente
Os tamanhos do WATCHMAN FLX variam de (20mm - 35mm)


INFORMAÇÃO PRIVILEGIADA:
Discussão do Ensaio Clínico PINNACLE FLX
Dr. Kenneth Stein, Vice Presidente Sênior, Diretor Médico de Controle de Ritmo na Boston Scientific
Dr. Ian Meredith, Vice Presidente Executivo, Diretor Médico Global da Boston Scientific
Dr. Ian Meredith, Vice Presidente Executivo, Diretor Médico Global da Boston Scientific